Задание 1
Осуществите реакции, характеризующие химические свойства:а) соляной кислоты (1-й вариант);б) раствора серной кислоты (2-й вариант).
Запишите уравнения проделанных вами реакций в молекулярной и ионной формах. Реакцию с металлом рассмотрите как окислительно-восстановительную.
1-й вариант. Свойства раствора соляной кислоты.
1. Взаимодействие с металлами, стоящими в электрохимическом ряду металлов до водорода с образованием соли и выделением газообразного водорода:
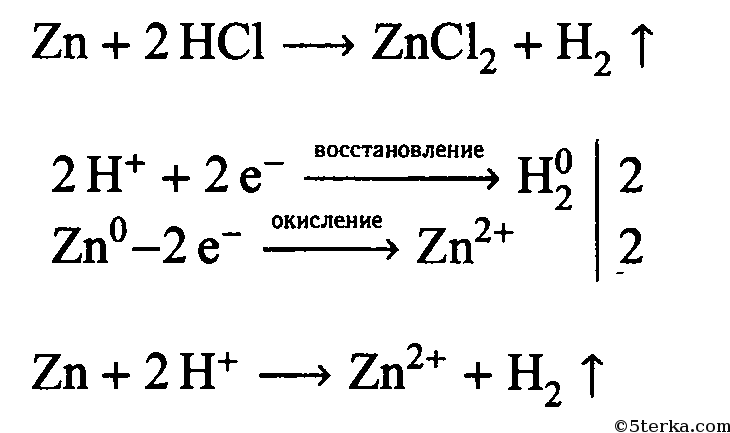
2. Взаимодействие с оксидами металлов с образованием растворимой соли и воды:
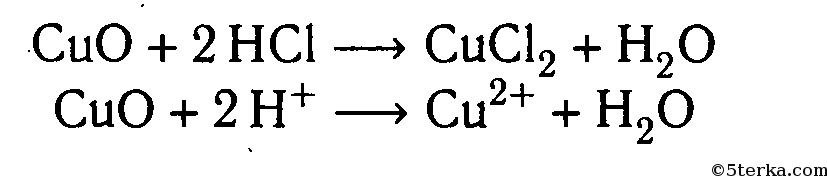
3. Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):

4. Взаимодействие с солями металлов, образованных более слабыми кислотами, например угольной:
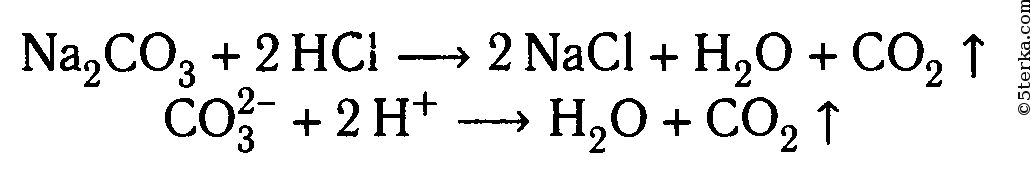
5. Взаимодействие с нитратом серебра с образованием нерастворимого осадка:

2-й вариант. Свойства раствора серной кислоты.
1. Взаимодействие с металлами, стоящими в электрохимическом ряду металлов до водорода:

2. Взаимодействие с оксидами металлов:
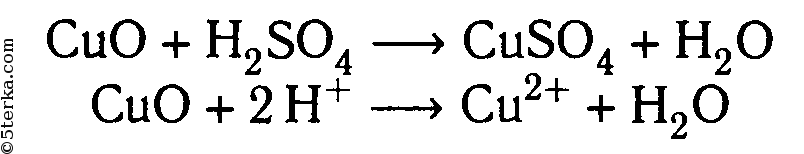
3. Взаимодействие с гидроксидами металлов (реакция нейтрализации):

4. Взаимодействие с солями металлов, образованных более слабыми кислотами:

5. Взаимодействие с хлоридом бария с образованием нерастворимого осадка:
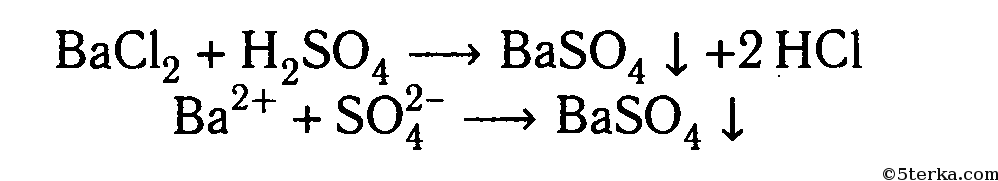
Задание 2
Проделайте реакции, характеризующие химические свойства раствора гидроксида натрия (1-й вариант).
Получите гидроксид железа (III) реакцией обмена и осуществите реакции, характеризующие его химические свойства (2-й вариант).
Запишите уравнения проделанных вами реакций в молекулярной и ионной формах.
1-й вариант. Свойства раствора гидроксида натрия.
1. Реакция нейтрализации:

2. Реакция обмена с солями в растворе:

2-й вариант.
Получение гидроксида железа (III).

Свойства гидроксида железа (III). 1. Реакция нейтрализации:

2. Реакция разложения:

Задание 3
Получите оксид серы (IV) и проделайте реакции, характеризующие его химические свойства (1-й вариант).
Проделайте реакции, характеризующие химические свойства оксида кальция (2-й вариант).
Запишите уравнения реакций в молекулярной и ионной формах, если это возможно.
1-й вариант.
Получение оксида серы (IV).
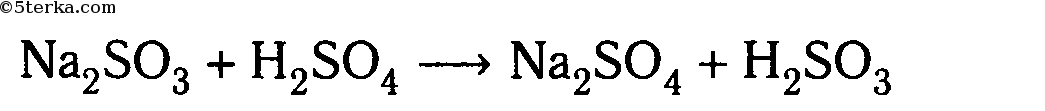
Свойства оксида серы (IV).
1. Растворяется в воде с образованием сернистой кислоты:
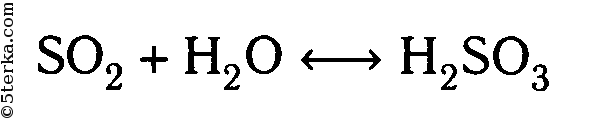
2. Взаимодействие со щелочами:

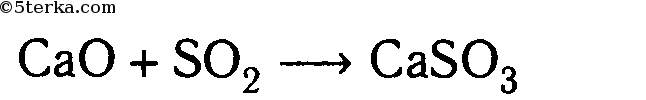
3. Взаимодействие с основными оксидами:
3. Обесцвечивает раствор перманганата калия.

2-й вариант. Свойства оксида кальция.
1. Растворение в воде:

2. Взаимодействие с кислотными оксидами:

3. Взаимодействие с кислотами:

Задание 4
Проделайте реакции, характеризующие химические свойства:а) хлорида железа (II) (1-й вариант);б) хлорида меди (II) (2-й вариант).
Запишите уравнения реакций в молекулярной и ионной формах. Реакции с участием металла рассмотрите как окислительно-восстановительные.
1-й вариант. Свойства хлорида железа (II).
1. Взаимодействие с щелочами:

2. Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений металлов левее железа:

3. Реакции ионного обмена с другими солями:
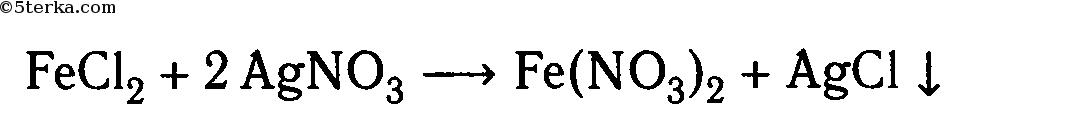
4. Образование сульфидов:

2-й вариант. Свойства хлорида меди (II).
1. Взаимодействие с щелочами:
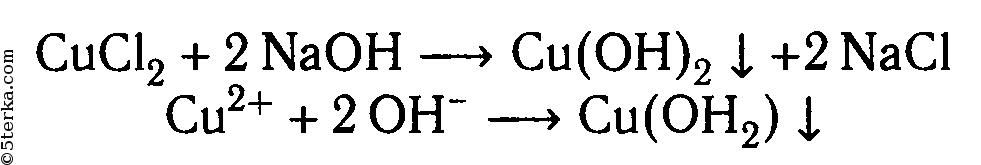
2. Взаимодействие с металлами, стоящими в электрохимическом ряду напряжений металлов левее меди:

3. Реакции ионного обмена с другими солями:

4. Образование сульфидов:

 Решебник
по
химии
за 8 класс (О.С.Габриелян, 2011 год),
Решебник
по
химии
за 8 класс (О.С.Габриелян, 2011 год),
задача №3
к главе «Глава 7. Свойства электролитов».