Опыт 1
Возьмите три пробирки и налейте в каждую по 2—3 мл раствора: в 1-ю — сульфата меди (II), во 2-ю — хлорида калия, в 3-ю — сульфата алюминия. Затем в каждую пробирку добавьте: в 1-ю немного раствора гидроксида натрия, во 2-ю — раствора фосфата натрия, а в 3-ю — раствора хлорида бария. Что наблюдаете?
Составьте молекулярные и ионные уравнения реакций. Сделайте вывод.
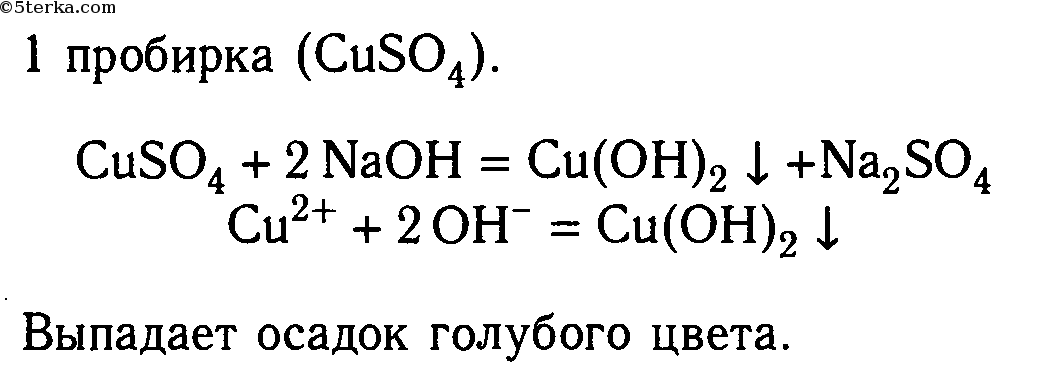

Вывод: если выпадает осадок, то реакции идут до конца.
Опыт 2
В две пробирки налейте по 2—3 мл растворов сульфита натрия и карбоната натрия соответственно. Затем прилейте в каждую из них раствор азотной кислоты. Что наблюдаете?
Составьте молекулярные и ионные уравнения реакций. Сделайте вывод.
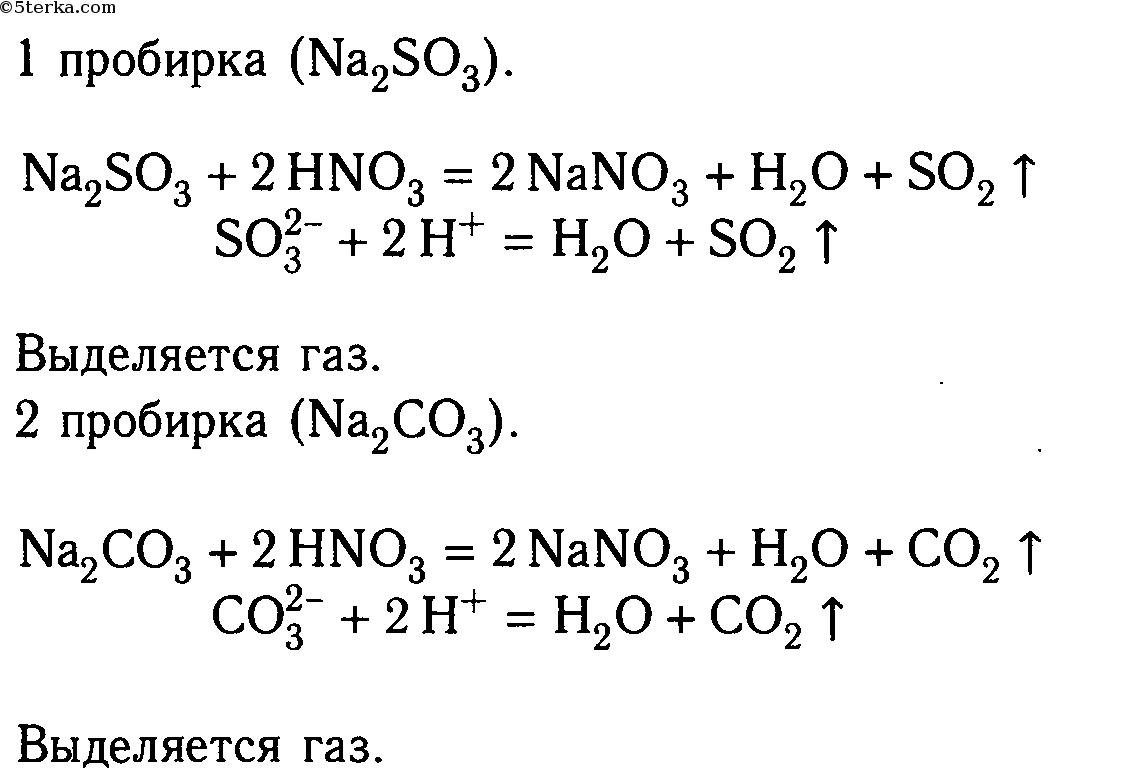
Вывод 1: если выделяется газ, то реакции идут до конца.
Вывод 2: угольная и сернистая кислоты неустойчивы.
Опыт 3
В одну пробирку налейте 3—4 мл раствора гидроксида натрия и добавьте две-три капли фенолфталеина. Раствор приобретает малиновый цвет. Затем прилейте соляную кислоту или раствор серной кислоты до обесцвечивания.
В другую пробирку налейте примерно 2—3 мл сульфата меди (II) и добавьте немного раствора гидроксида натрия. Образуется голубой осадок гидроксида меди (II). Прилейте в пробирку серную кислоту до растворения осадка Составьте уравнения происходящих реакций в молекулярном и ионном виде. Поясните, почему в первой пробирке произошло обесцвечивание, а во второй — растворение осадка. Каким общим свойством обладают растворимые и нерастворимые основания?

Осадок гидроксида меди растворился так как сульфат меди растворимое соединение.
Растворимые и нерастворимые в воде основания можно растворить в растворах кислот, Происходит реакция нейтрализации.
 Решебник
по
химии
за 8 класс (О.С.Габриелян, 2011 год),
Решебник
по
химии
за 8 класс (О.С.Габриелян, 2011 год),
задача №2
к главе «Глава 7. Свойства электролитов».