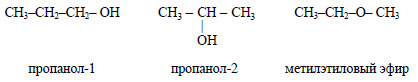1) Все атомы, входящие в молекулы органических веществ, соединены в определенной последовательности.
Очевидно, что для любого вещества можно изобразить структурную формулу. Нарисуем структурные формулы этана, пропилена и бензола:
2) Свойства веществ зависят не только от состава (то есть от того, какие атомы входят в состав молекулы), но и от строения (то есть от того, как именно они соединены).
Несколько веществ с одинаковой молекулярной формулой могут иметь различное строение. Например, формуле C3H8O соответствует три изомера – пропанол-1, пропанол-2 и метилэтиловый эфир:
Формуле C2H7N соответствуют этиламин и диметиламин:
3) По свойствам вещества можно объяснить его строение, а по строению – предвидеть свойства.
Например, карбоновые кислоты содержат карбоксильную группу, и можно предвидеть, что атом водорода карбоксильной группы будет замещаться на атом металла при реакции с основаниями. С другой стороны, если известен факт, что карбоновые кислоты реагируют с основаниями, это можно объяснить присутствием в молекуле карбоксильной группы.
В молекулах алкенов есть двойная связь. Присоединение к алкенам брома объясняется именно наличием в молекуле двойной связи. С другой стороны, если в молекуле есть двойная связь, то можно предвидеть, что вещество будет реагировать с бромом.
4) Атомы и группы атомов в молекулах влияют друг на друга.
В молекуле фенола происходит смещение электронов от атома кислорода к бензольному кольцу, и вследствие этого электроны атома водорода в большей степени смещаются к атому кислорода. Связь между атомами водорода и кислорода становится более полярной и поэтому разрывается легче, чем в спиртах. Атом водорода в фенолах легче замещается на металл, чем в спиртах, то есть является более подвижным.
Хлоруксусная кислота сильнее, чем уксусная кислота. Электроотрицательность атома хлора выше, чем атома углерода. Поэтому хлор оттягивает на себя электроны, участвующие в образовании химической связи между атомами хлора и кислорода. Этот эффект смещения электронной плотности передается по цепочке химических связей к ОН-группе. В результате связь О–Н в карбоксильной группе становится более полярной и поэтому легче разрывается. В результате хлоруксусная кислота диссоциирует на ионы легче, чем уксусная кислота, то есть является более сильной кислотой.
 Решебник
по
химии
за 11 класс (Г.Е. Рудзитис, Ф.Г. Фельдман, 2000 год),
Решебник
по
химии
за 11 класс (Г.Е. Рудзитис, Ф.Г. Фельдман, 2000 год),
задача №1
к главе «Глава XIV. Обобщение знаний по курсу органической химии».