Задания. 1. Проведите качественную реакцию на карбо-нат-ион.
2. Осуществите превращения гидрокарбоната кальция в карбонат кальция и наоборот.
3. Изучите гидролиз карбоната натрия.
4. Проведите реакцию между растворами карбоната натрия и хлорида кальция. Исследуйте продукты реакции с помощью азотной кислоты.
Соблюдайте правила техники безопасности при проведении опытов!
Оборудование. Лабораторный штатив, штатив с пробирками, детали прибора для разложения гидрокарбоната натрия, нагревательный прибор.
Вещества. Растворы азотной и соляной кислот (10%-е), карбоната натрия и хлорида кальция (10% -е), фенолфталеина, известковой воды, гидрокарбоната кальция; кристаллический гидрокарбонат натрия, кусочек мела или мрамора.
Выполнение опыта
1. В одну пробирку поместите небольшой кусочек мела или мрамора, в другую налейте 1 мл раствора карбоната натрия. В обе пробирки добавьте (не более 1 мл) раствора соляной кислоты. Что вы наблюдаете? Внесите в обе пробирки зажженные спички. Наличие какого газа вы обнаружили? Напишите полные и сокращенные ионные уравнения реакций и сделайте вывод, какое вещество может быть использовано для обнаружения карбонат-иона.
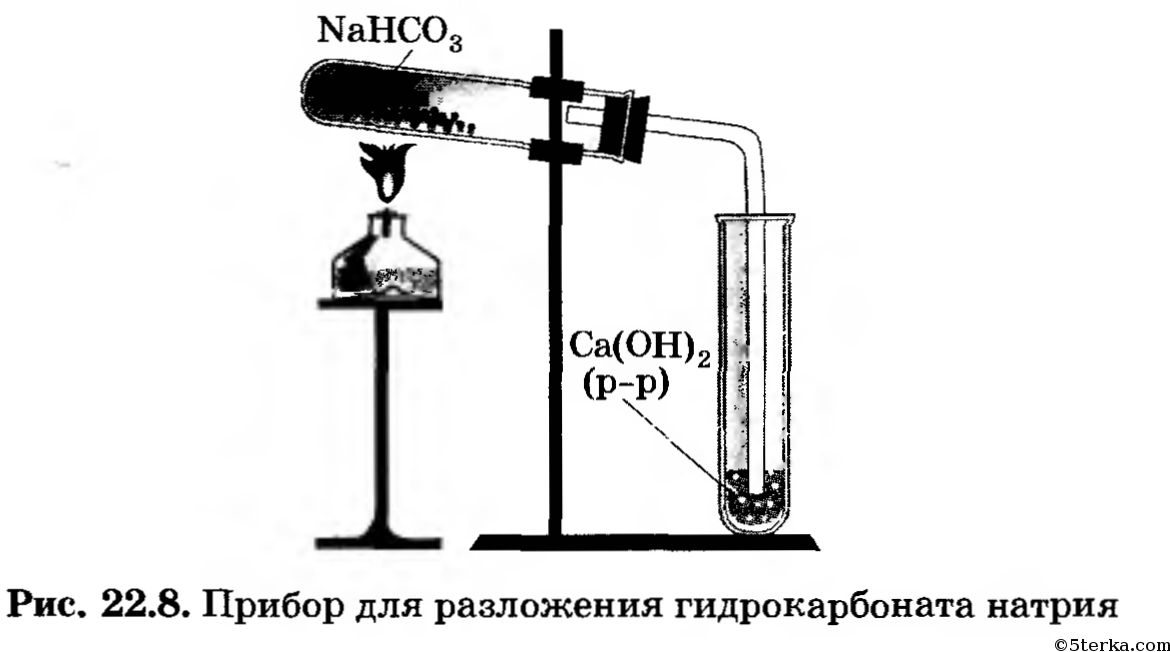
2. а) Налейте в пробирку 2 мл раствора гидрокарбоната кальция и добавьте к нему немного известковой воды. Что вы наблюдаете? Составьте полное и сокращенное ионные уравнения этой реакции.б) Соберите прибор, как показано на рисунке 22.8. Насыпьте в пробирку гидрокарбонат натрия. Закройте ее пробкой с газоотводной трубкой и закрепите прибор в штативе так, чтобы отверстие пробирки было ниже ее дна, а конец газоотводной трубки почти доставал дна пробирки с известковой водой. Начинайте нагревать гидрокарбонат натрия в пробирке.
Наблюдайте за изменениями, происходящими в обеих пробирках. Как только известковая вода помутнеет, поднимите
лапку штатива вместе с пробиркой и газоотводной трубкой вверх и только после этого прекратите нагревание. Объясните необходимость такого порядка действий при проведении данного опыта.
Какие вещества образуются при нагревании гидрокарбоната натрия? Составьте уравнение данной реакции и сделайте вывод о химизме превращения гидрокарбонатов в карбонаты.
3. В пробирку налейте по 1 мл раствора карбоната натрия и добавьте по 2—3 капли фенолфталеина. Что вы наблюдаете? Объясните с помощью ионных уравнений реакций результат опыта.
4. В пробирку налейте 1 мл раствора карбоната натрия, столько же раствора хлорида кальция. Что вы наблюдаете? Ответ поясните ионными уравнениями реакций.
К получившемуся осадку прилейте немного (0,5 мл) раствора азотной кислоты. Какой газ выделяется? Объясните причину его выделения с помощью ионных уравнений реакции.
1.

2.
Проведем несколько опытов:
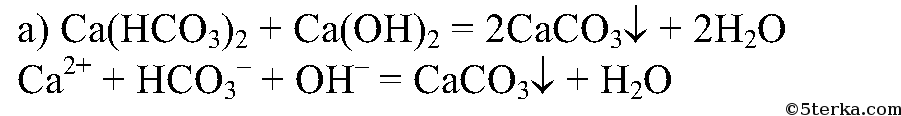
Выпадает белый осадок.
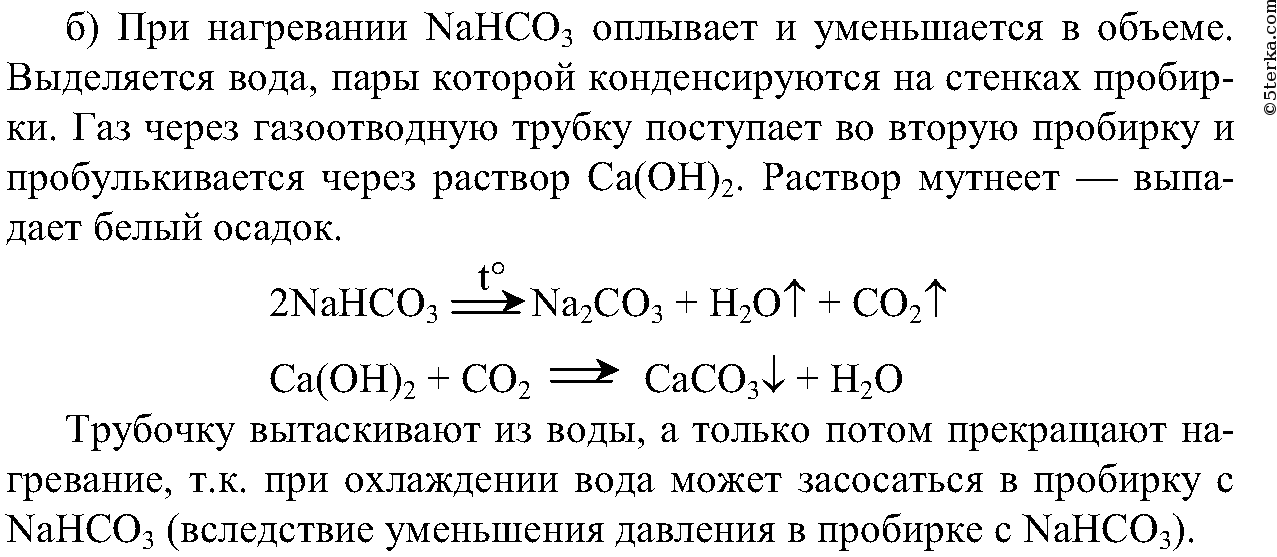
Вывод: карбонаты можно получить, прокаливая гидрокарбонаты. 3.

Мел плохо растворяется, и в пробирке ничего не происходит.
4.
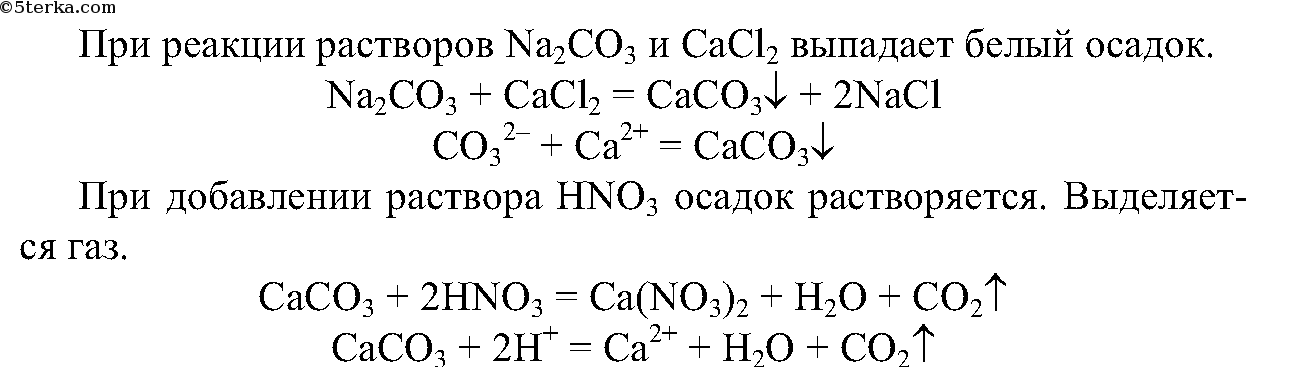
 Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
задача №9
к главе «Лабораторные работы и опыты».