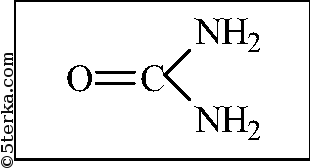
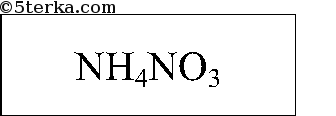Задания. 1. Изучите некоторые физические свойства образцов азотных удобрений.
2. Проделайте качественную реакцию на нитрат-ион.
3. Распознайте ион аммония.
Соблюдайте правила техники безопасности при работе с кислотами и нагревательными приборами!
Оборудование. Штатив с пробирками, шпатель, нагревательные приборы, держатель для пробирок.
Вещества. Набор азотных удобрений: аммиачная и натриевая селитры, сульфат аммония, мочевина; раствор гидроксида натрия, медные опилки или проволока, концентрированная серная кислота, дистиллированная вода, вода (в стакане).
Выполнение опыта
1. Исследуйте физические свойства выданных вам образцов азотных удобрений: цвет, агрегатное состояние, растворимость в воде. Для определения растворимости налейте в пробирку не более 1/4 ее объема дистиллированной воды и вносите удобрение небольшими порциями, постоянно перемешивая. Результаты исследования внесите в таблицу:
2. В сухую пробирку насыпьте аммиачную селитру (объемом с горошину), затем внесите немного медных опилок (или опустите медную проволоку) и добавьте несколько капель концентрированной серной кислоты. Что вы наблюдаете? Если после добавления серной кислоты бурый газ не появится, смесь слегка нагрейте. Как только появится бурое облачко, прекратите реакцию, опрокинув пробирку в стакан с водой. Наличие каких ионов в аммиачной селитре подтверждает эта реакция? Какое из выданных вам удобрений дает такую же реакцию? Составьте уравнение реакции.
3. Налейте в пробирку 2 мл приготовленного вами раствора аммиачной селитры, добавьте столько же раствора гидроксида натрия, нагрейте, по запаху и изменению окраски фиолетовой лакмусовой бумажки распознайте газообразный продукт реакции.
Напишите уравнения проведенных реакций.
1.
Составим предложенную таблицу
2.
Часть опилок в опыте растворяется, слышно шипение, появляется бурое облачко, пробирка заметно нагревается.

3.
При нагревании начинает выделяться газ с резким характерным запахом. Лакмус окрашивается в синий цвет. Этот газ аммиак.
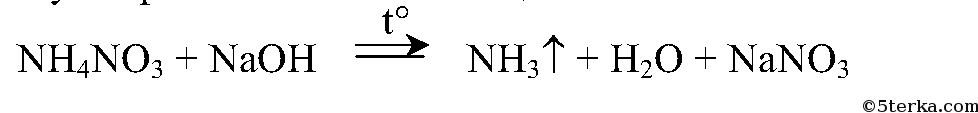
 Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
задача №7
к главе «Лабораторные работы и опыты».