Сжигание железа в кислороде и хлоре.
1. Кислород окисляет железо, при этом происходит образование железной окалины - смешанного оксида
Хлор является сильным окислителем, поэтому окисляет железо до более высокой степени окисления (+3), при этом образуется хлорид желез (III). 2. Кислород и хлор- окислители, железо - восстановитель.
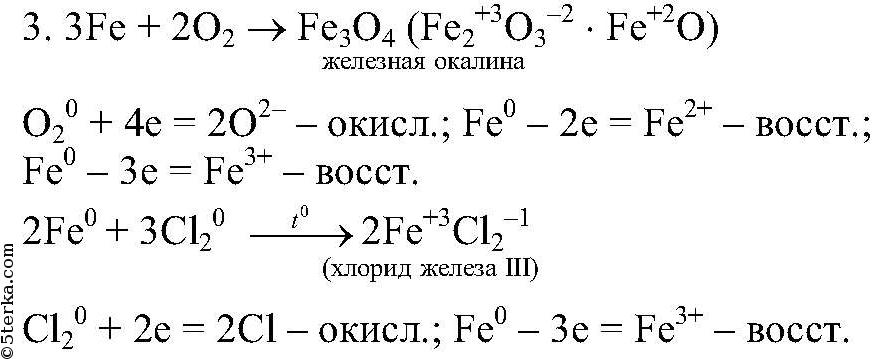
Взаимодействие железа с концентрированными кислотами 1. Азотная и концентрированная серная кислоты относятся к ки-слотам-окислителям, т.е. они проявляют сильные окислительные свойств за счет кислотного остатка. Выделяющийся при восстановлении азотной кислоты оксид азота(II) легко окисляется кислородом воздух до оксида азота (IV).
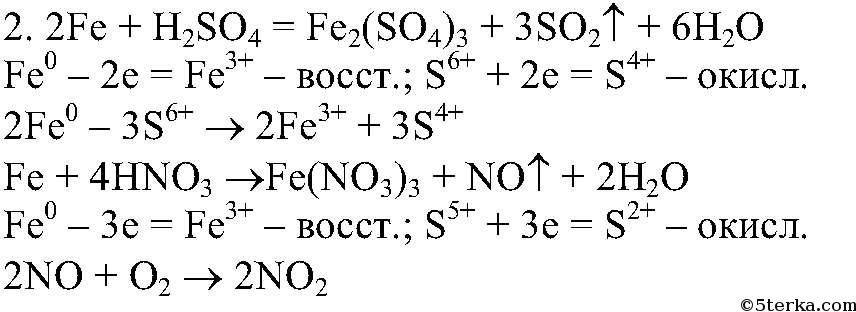
Примечание: с концентрированной азотной кислотой и концентри-рованной серной на холоду железо не реагирует (пассивируется).
Получение гидроксида железа (II) и взаимодействия его с кислотами
а) Действия: К свежеприготовленному раствору сульфата железа (II) добавляем раствор гидроксида натрия. Наблюдения: Образуется осадок зеленоватого цвета. Уравнения реакции: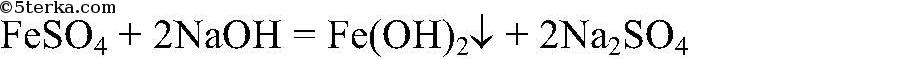
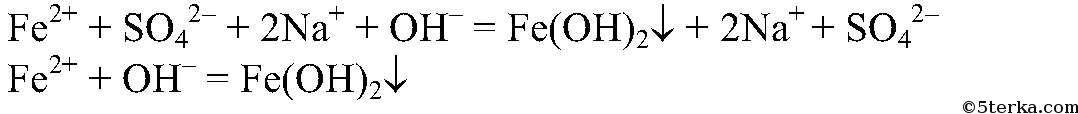
Выводы: Гидроксиды железа (II) и (III) можно получить в резуль-тате реакции обмена между растворимыми солями желез (II) и (III) раствором щелочи, т.к. в этом случае происходит связывание ионов:

б) Действия: К осадку добавляем раствор соляной кислоты. Наблюдения: Осадок растворяется. Уравнения реакции:

Выводы: Т.к.

имеет основной характер, поэтому он реагирует с кислотами.
Получение солей гидроксида железа (III) и взаимодействия его с кислотами с образованием соответствующих солей
а) Действия: К р-ру хлорида железа (III) добавляем р-р щелочи. Наблюдения: Выпадает осадок бурого цвета. Уравнения реакции: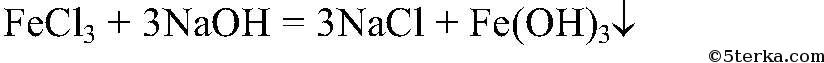

Выводы: Ионы

можно определить с помощью реакции между их солями и щелочью, т.к. в этом случае образуются осадки:

- зеленый;

- бурый. б) Действия: К осадку добавляем серную кислоту. Наблюдения: Осадок растворяется. Уравнения реакции:


Источник:
 Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №0
к главе «Лабораторные и практические работы».
Комментарии