1) Получение оксида углерода (IV) и определение его свойств
а) Действия: В пробирку кладем несколько кусочков мрамора, добавляем раствор соляной кислоты. Наблюдения: Выделяется газ. Уравнения реакции:
Выводы: При действии на мрамор соляной кислотой, она вытесняет из карбоната слабую угольную кислоту, которая затем разлагается на H2O и CO2
б) Действия: Конец газоотводной трубки помещаем в пробирку с известковой водой. Наблюдения: Образуется белый осадок, который растворяется. Уравнения реакции:
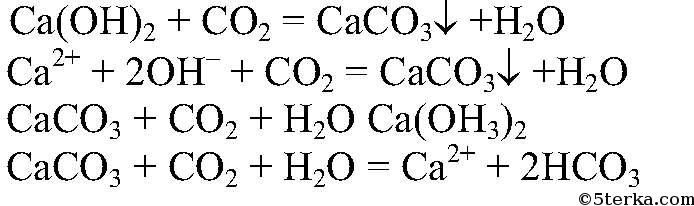
Выводы: При пропускании углекислого газа через известковую воду образуется карбонат кальция, который затем растворяется, превращаясь в гидрокарбонат. в) Действия: Пропускаем углекислый газ через дистиллированную воду. Затем добавляем синий лакмус. Наблюдения: Лакмус краснеет. Уравнения реакции:
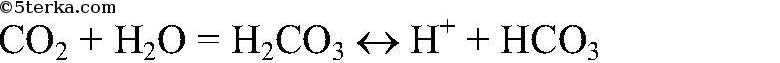
Выводы: Т.к. синий лакмус краснеет, следовательно, при растворении в воде образуется кислота. г) Действия: Наливаем в пробирку разбавленный

добавляем фенолфталеин и пропускаем углекислый газ. Наблюдения: В растворе щелочи фенолфталеин розовеет, при пропускании углекислого газа - обесцвечивается. Уравнения реакции:


Выводы: Идет реакция между

Это еще раз подтверждает кислотные свойства
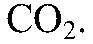
2) Распознавание карбонатов.
Даны вещества:
а) Действия: Ко всем веществам добавляем соляную кислоту. Наблюдения: В одной из пробирок выделяется газ. Уравнения реакции:
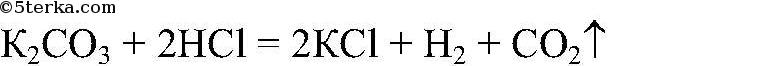

Выводы: В данной пробирке - карбонат калия, это качественная реакция на карбонат-ион. б) Наблюдения: В другой пробирке образ. прозрачный осадок. Уравнения реакции:
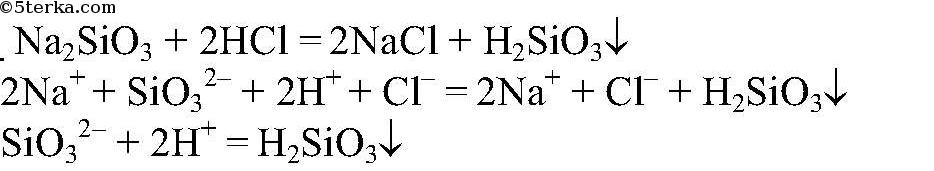
Выводы: В данной пробирке - силикат натрия, т.к. происходит образование нерастворимой кремниевой кислоты. в) Действия: Два оставшихся вещества растворяем водой и добавляем раствор хлорида бария. Наблюдения: В одной из пробирок образовался белый осадок. Уравнения реакции:


Выводы: Это качественная реакция на сульфат-ион, значит, в данной пробирке находится сульфат натрия. г) Действия: В оставшийся р-р добавляем р-р нитрата серебра (I). Наблюдения: Образовался белый осадок. Уравнения реакции:


Выводы: Реакция является качественной на хлорид-ион, следовательно, в данной пробирке - хлорид цинка.
Источник:
 Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №0
к главе «Лабораторные и практические работы».
Комментарии