
Осадок образуется в результате связывания ионов
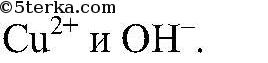
Осадок вместо раствора

можно взять раствор любой щелочи или растворимых соединений барий. Например:
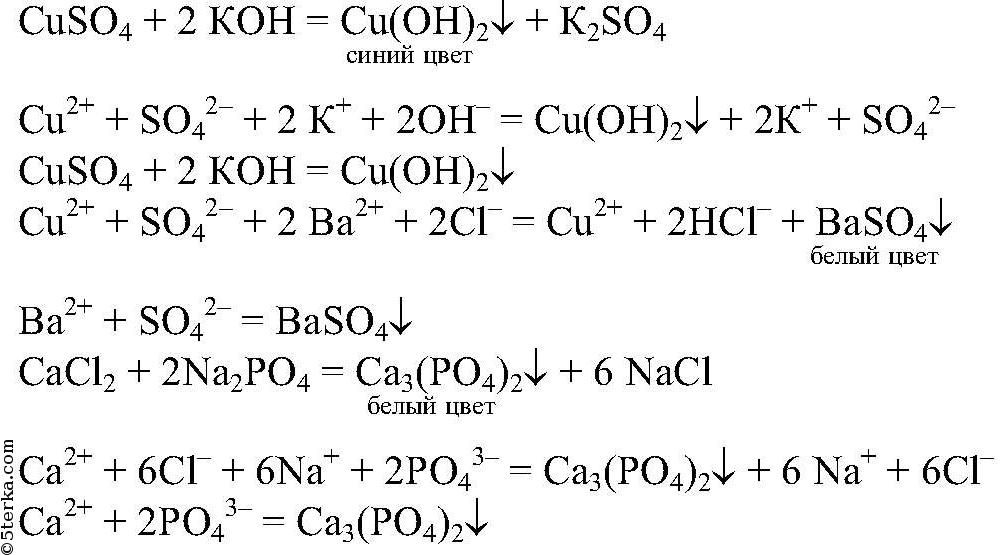
Осадок образуется в результате связывания ионов
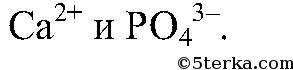
Вместо раствора
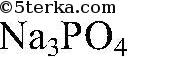
можно взять раствор

или

а также

или

Например:

Осадок образуется в результате связывания ионов
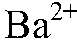
и
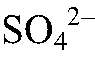
Вместо раствора

можно взять любое растворимое соединение бария или щелочь. Например:

2) Реакции, идущие с выделением газа.
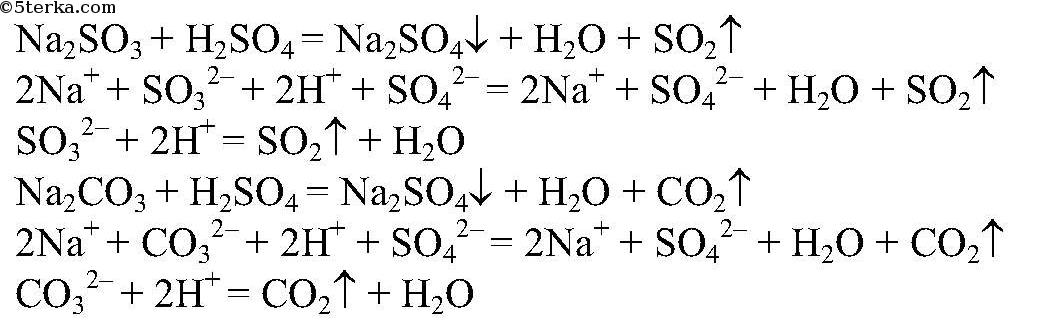
На данные растворы можно было бы подействовать любой более сильной кислотой, например:

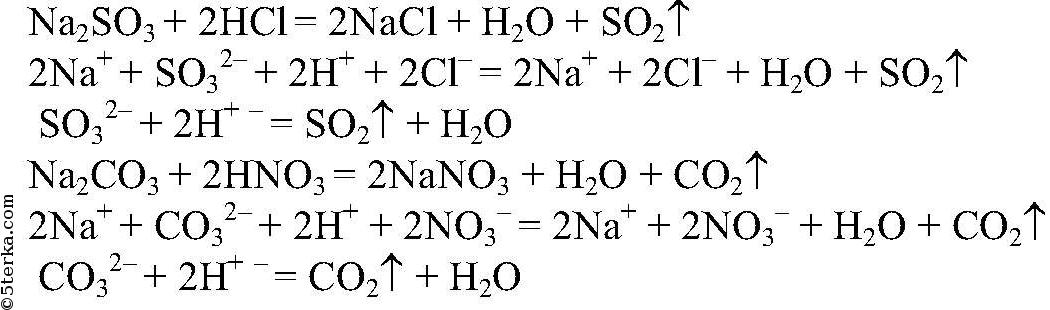
3)Реакции, идущие с образованием малодиссоциирующего вещества.

Растворение осадка (гидрооксида меди) происходит под действиям ионов
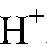
которые более прочно связаны в случае воды, чем гидроксида меди (II). 4) Качественная реакция на хлорид-ион.
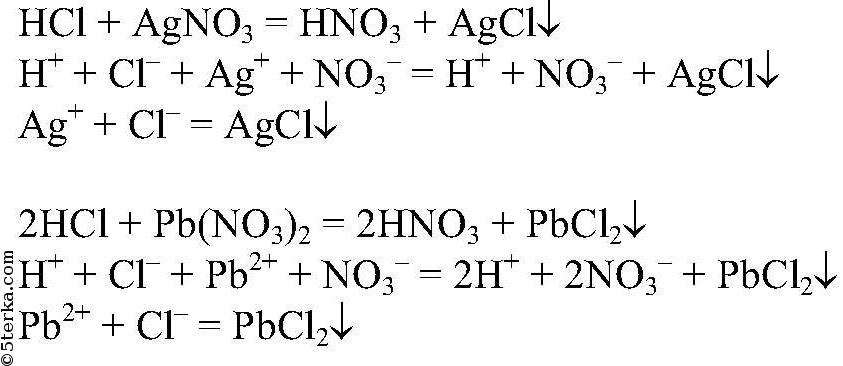
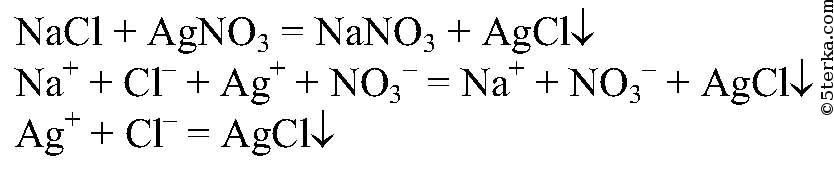


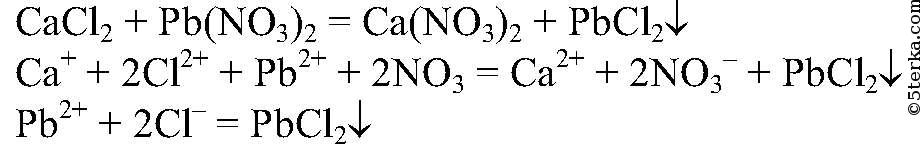
а) и б) Для распознавания соляной кислоты и ее солей можно использовать раствор нитрата серебра (I), т.к. при их взаимодействии образуется характерный белый осадок
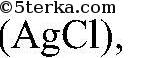
не растворяющийся даже в концентрированной азотной кислоте. Вместо нитрата серебра (I) можно использовать нитрат свинца (II), т.к. он дает такую же качественную реакцию с образованием белого осадка
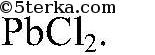
Растворы хлоридов от соляной кислоты можно отличить с помощью индикаторов, изменяющих свою окраску в присутствии ионов
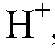
например: синего лакмуса, метилоранжа и др.
Источник:
 Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
Решебник
по
химии
за 9 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 1999 год),
задача №0
к главе «Лабораторные и практические работы».
Комментарии