3*. МГУ96. По данным электронографического эксперимента межъядерные расстояния в молекуле NF3 равны: r(N — F) = 0,137 нм, r(F—F) = 0,213 нм. Определите, какую геометрическую фигуру образуют ядра атомов в этой молекуле. Установите тип гибридизации центрального атома.
(См. ответ на задание 3 из Задачи к § 27.2.)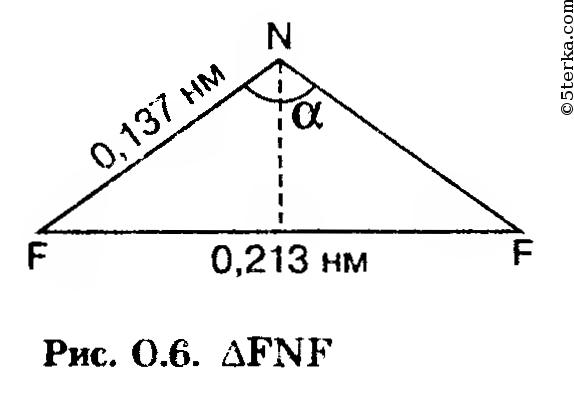
Электронная формула молекулы

показывает, что вокруг центрального атома имеется четыре максимума электронной плотности. Это значит, что угол между связями должен быть близок к тетраэдрическому, а молекула имеет форму треугольной пирамиды, в вершинах которой находятся атом азота и атомы фтора. Угол ∠FNF найдем из равнобедренного ΔFNF, показанного на рисунке 0.6:
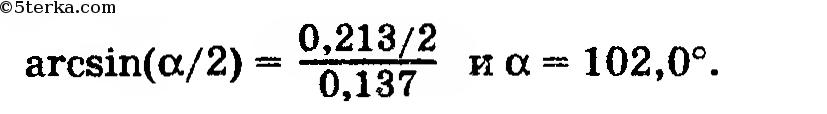
Источник:
 Решебник
по
химии
за 10 класс (Л.С. Гузей, Р.П. Суровцева, 1999 год),
Решебник
по
химии
за 10 класс (Л.С. Гузей, Р.П. Суровцева, 1999 год),
задача №3
к главе «Задачи к § 30.2».
Комментарии