Из всех компонентов газа горят метан, этан и пропан:
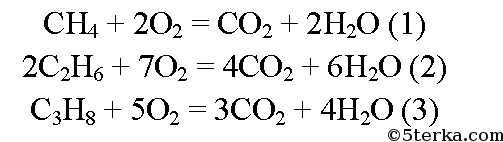
Вычислим объем метана, этана и пропана:
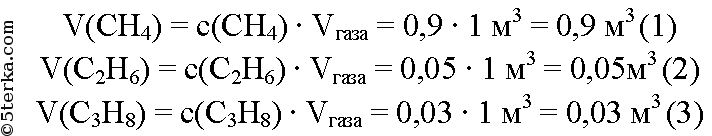
Для решения воспользуемся следствием из закона Авогадро: объемные соотношения газов равны их мольным соотношениям. По уравнению реакции (1) для сжигания 1 моль метана необходимо 2 моль кислорода. Пусть для сжигания 0,9 м3 метана нужно х м3 кислорода. Составим пропорцию:
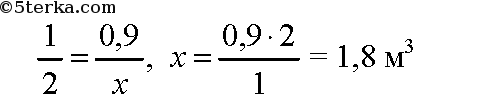
По уравнению реакции (2) для сжигания 2 моль этана необходимо 7 моль кислорода. Пусть для сжигания 0,05 м3 этана нужно у м3 кислорода. Составим пропорцию:
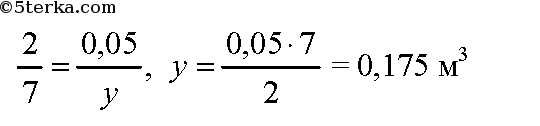
По уравнению реакции (3) для сжигания 1 моль пропана необходимо 5 моль кислорода. Пусть для сжигания 0,03 м3 пропана нужно z м3 кислорода. Составим пропорцию:
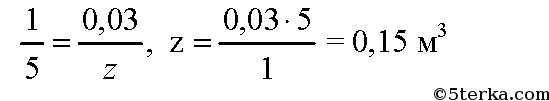
Таким образом, для сжигания газа необходимо 1,8 + 0,175 + 0,15 = 2,125 м3 кислорода. В воздухе содержится примерно 21% кислорода по объему, или 0,21. Вычислим объем воздуха, необходимый для сжигания газа:
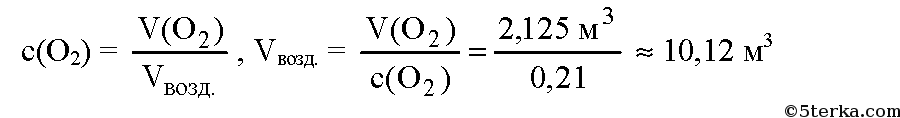
Ответ: необходимо 10,12 м3 воздуха.
 Решебник
по
химии
за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),
Решебник
по
химии
за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),
задача №1
к главе «Глава VI. Природные источники углеводородов и их переработка. §§1-5 (стр. 74) Задачи».