Структурная формула о-ксилола:
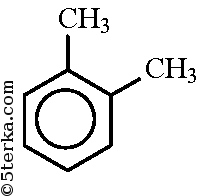
Молекулярная формула о-ксилола C8H10. Уравнение реакции горения ксилола:
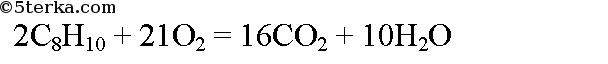
Вычислим молярную массу о-ксилола:
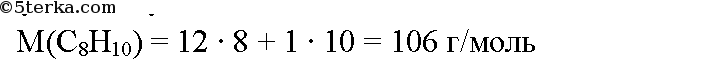
Вычислим количество вещества о-ксилола:
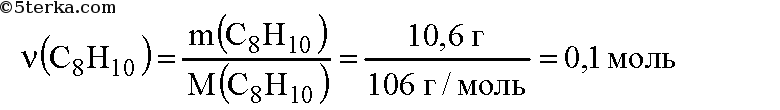
По уравнению реакции из 2 моль ксилола получается 16 моль оксида углерода. Пусть из 0,1 моль ксилола получится х моль оксида углерода. Составим пропорцию:
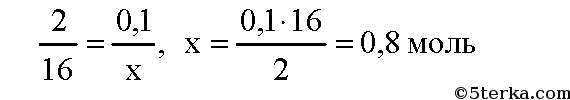
Вычислим массу гидроксида натрия в растворе:
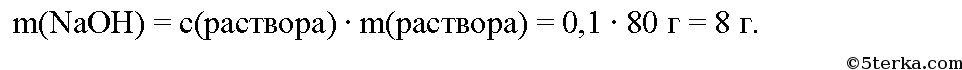
Вычислим молярную массу гидроксида натрия:
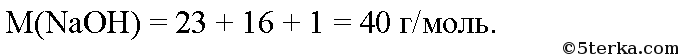
Вычислим количество вещества гидроксида натрия:
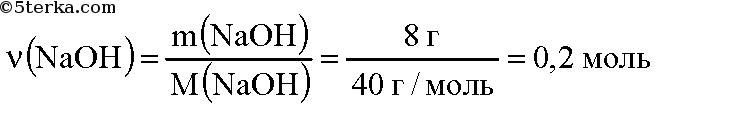
При пропускании через раствор гидроксида натрия оксида углерода может образоваться либо карбонат, либо гидрокарбонат натрия:
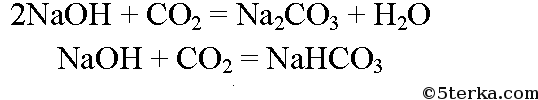
Для образования средней соли, карбоната натрия, необходимо 2 моль гидроксида натрия на 1 моль оксида углерода. Для образования кислой соли, гидрокарбоната натрия, нужно 1 моль гидроксида натрия на 1 моль оксида углерода (IV). По условию получается, что на 0,8 моль оксида углерода приходится 0,2 моль гидроксида натрия, то есть на 1 моль гидроксида натрия приходится 4 моль оксида углерода. Значит, оксид углерода находится в избытке даже для образования кислой соли. Образуется гидрокарбонат натрия, расчет его количества ведем по количеству гидроксида натрия. По уравнению из 1 моль гидроксида натрия образуется 1 моль гидрокарбоната натрия, значит из 0,2 моль гидроксида натрия получится 0,2 моль гидрокарбоната натрия. Вычислим молярную массу гидрокарбоната натрия.
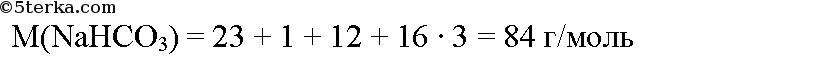
Вычислим массу гидрокарбоната натрия:
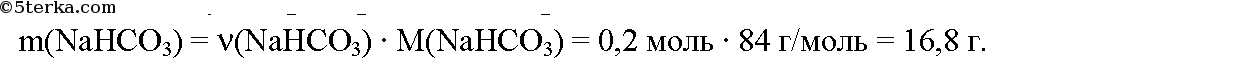
Ответ: образовалось 16,8 г гидрокарбоната натрия NaHCO3.
 Решебник
по
химии
за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),
Решебник
по
химии
за 10 класс (Г.Е.Рудзитис, Ф.Г.Фельдман, 2000 год),
задача №3
к главе «Глава V. Ароматические углеводороды (арены) (стр. 64) Задачи».