Задание. Распознайте сульфат натрия с помощью качественной реакции.
Соблюдайте правила техники безопасности при работе с кислотами!
Оборудование. Штатив с пробирками.
Вещества. 5% -е растворы сульфата, хлорида и нитрата натрия, 10% -е растворы хлорида бария, серной, соляной и азотной кислот, порошок медного купороса, вода (в стакане).
Выполнение опыта
1. В три пробирки налейте по 1 мл растворов сульфата натрия, хлорида натрия и нитрата натрия. В каждую из этих пробирок добавьте немного хлорида бария. Что вы наблюдаете?
Составьте полные и сокращенные ионные уравнения наблюдаемых реакций.
2. Докажите, что выданные вам голубые кристаллы содержат сульфат меди (II). Составьте уравнения реакций.
3. Налейте в три пробирки серную, азотную и соляную кислоты, добавьте в них раствор хлорида бария. Что вы наблюдаете? Напишите уравнения реакций.
Сделайте общий вывод, с помощью какого реактива можно распознать сульфат-ионы.
1.
Наблюдается появление белого осадка в пробирке с сульфатом натрия. В других пробирках видимых изменений не наблюдается.
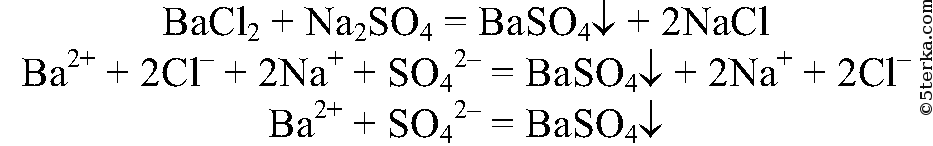
2.

3.
В пробирке с серной кислотой выпадет белый осадок. В других пробирках ничего не происходит.
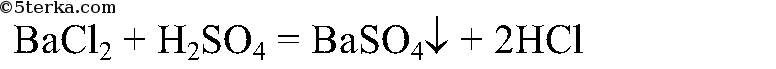
Вывод: сульфат-ионы распознаются с помощью растворимых солей бария.
 Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
Решебник
по
химии
за 9 класс (Л.С.Гузей, В.В.Сорокин, Р.П.Суровцева, 2000 год),
задача №5
к главе «Лабораторные работы и опыты».