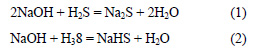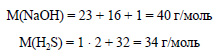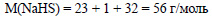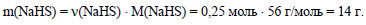Решение:
Возможно образование двух солей – сульфида натрия по уравнению (1) и гидросульфида натрия по уравнению (2).
Вычислим молярные массы гидроксида натрия и сероводорода:
Вычислим количество вещества гидроксида натрия и сероводорода:
По уравнению (2) 1 моль гидроксида натрия реагирует с 1 моль сероводорода, значит для реакции с 0,59 моль сероводорода нужно 0,59 моль гидроксида натрия, а по условию взяли только 0,25 моль. Следовательно, сероводород взят в избытке, и образуется гидросульфид натрия, расчет ведем по гидроксиду натрия. Из 1 моль гидроксида натрия по уравнению образуется 1 моль гидросульфида натрия, следовательно из 0,25 моль гидроксида натрия получится 0,25 моль гидросульфида натрия.
Вычислим молярную массу гидросульфида натрия:
Вычислим массу гидросульфида натрия:
Ответ: получится 0,25 моль (14 г) гидросульфида натрия.
 Решебник
по
химии
за 11 класс (Г.Е. Рудзитис, Ф.Г. Фельдман, 2000 год),
Решебник
по
химии
за 11 класс (Г.Е. Рудзитис, Ф.Г. Фельдман, 2000 год),
задача №2
к главе «Глава II. Периодический закон и периодическая система Д.И. Менделеева на основе учения о строении атома».