Фазовый переход из газообразного состояния в жидкое возможен, если средняя потенциальная энергия притяжения молекул превышает их среднюю кинетическую энергию. Для этого температура газообразного состояния (пара) должна быть ниже некоторой критической температуры. Критическая температура — максимальная температура, при которой пар можно превратить в жидкость.
Конденсация — явление перехода пара из газообразного состояния в жидкое.
Испарение — парообразование со свободной поверхности жидкости. При испарении жидкость охлаждается, поэтому для поддержания постоянной температуры к ней нужно подводить количество теплоты, пропорциональное массе испаряющихся молекул:
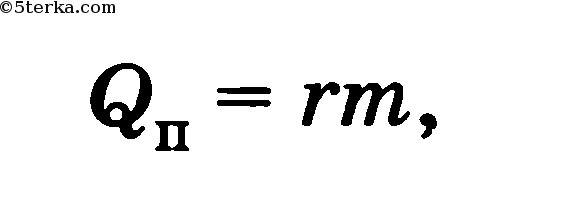
где r — удельная теплота парообразования.
Единица количества теплоты — джоуль (Дж).
Количество теплоты, получаемое жидкостью при конденсации, равно количеству теплоты, теряемому при ее испарении
В равновесии число молекул пара, конденсирующихся за определенный промежуток времени, равно числу молекул жидкости, испаряющихся с ее поверхности за это же время. Насыщенный пар — пар, находящийся в термодинамическом равновесии со своей жидкостью. Давление насыщенного пара при данной температуре — максимальное давление, которое может иметь пар над жидкостью при этой температуре.
Давление насыщенного пара возрастает при увеличении температуры жидкости.
Относительная влажность воздуха — процентное отношение концентрации водяного пара в воздухе к концентрации насыщенного пара при той же температуре.
Кипение — парообразование, происходящее во всем объеме жидкости при определенной температуре. Температура кипения — температура, при которой давление насыщенного пара жидкости (внутри пузырьков) начинает превосходить внешнее давление на жидкость. Температура кипения жидкости зависит от внешнего давления и остается постоянной в процессе кипения. Поверхностное натяжение — явление молекулярного давления на жидкость, вызванное притяжением молекул поверхностного слоя к молекулам внутри жидкости. Поверхностная энергия — дополнительная потенциальная энергия молекул поверхностного слоя жидкости.
Сила поверхностного натяжения — сила, направленная по касательной к поверхности жидкости, перпендикулярно участку контура, ограничивающего поверхность, в сторону ее сокращения:
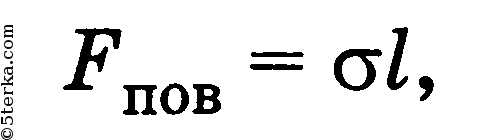
где l — длина участка поверхностного слоя, σ — поверхностное натяжение.
Единица поверхностного натяжения — ньютон на метр (Н/м). Смачивание — искривление поверхности жидкости у поверхности твердого тела в результате взаимодействия молекул жидкости с молекулами твердого тела.
Жидкость смачивает поверхность, если силы притяжения между молекулами жидкости меньше сил притяжения между молекулами жидкости и твердого тела.
Жидкость не смачивает поверхность, если силы притяжения между молекулами жидкости больше сил притяжения между молекулами жидкости и твердого тела.
Мениск — форма поверхности жидкости вблизи стенки сосуда.
Угол смачивания — угол между плоскостью, касательной к поверхности жидкости и стенкой. Капиллярность — явление подъема или опускания жидкости в узких сосудах (капиллярах).
Высота подъема жидкости в капилляре обратно пропорциональна его радиусу r:
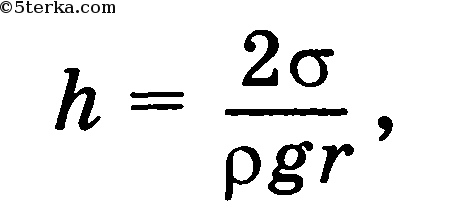
где а — поверхностное натяжение, р — плотность жидкости, g — ускорение свободного падения.